胰腺癌患者預后較差,80%以上的患者確診時無法行根治性手術,而且術后的復發轉移率也很高,因此化療是目前胰腺癌的主要治療選擇。但現有的標準化療方案帶來的獲益有限,仍需尋找新的治療手段。近年來,免疫治療已在多個瘤種中取得了令人矚目的成果,然而,胰腺癌免疫抑制性的腫瘤微環境限制了單純免疫治療的效果,針對胰腺癌免疫微環境的聯合治療策略,有望提高胰腺癌免疫治療的效果,為胰腺癌患者帶來新的治療選擇。
病例部分
病例來源:南京大學醫學院附屬鼓樓醫院胰腺腫瘤MDT團隊提供
基本病史:
患者男性,63歲。2020年6月12日因“上腹部不適半年余”就診。既往史:陳舊性肺結核、下肢靜脈血栓。體格檢查:無明顯異常。
輔助檢查:
腫瘤標志物:CA19-9:85.06U/ml,CA242:17.77U/mL,余(-)。
血常規、生化全套:無明顯異常。
腹部B超(2020-06-02):胰腺體部低回聲包塊。
腹部增強CT(2020-06-11):胰體部乏血供占位,胰腺癌可能。
治療前CT(2020-06-15):病灶長徑:32mm;侵犯門靜脈、腸系膜上靜脈及脾靜脈;無遠處轉移。
胰腺穿刺涂片(2020-06-19):查見癌細胞。
胰腺穿刺組織(2020-06-19):凝血塊內見極少量異型腺上皮細胞,具有中-重度異型性。
診斷:
胰腺癌(胰體部,交界可切除,合并門靜脈、腸系膜上靜脈及脾靜脈侵犯)
治療史:
患者于2020-06-23至2020-10-13行AG方案(白蛋白紫杉醇+吉西他濱)化療聯合替雷利珠單抗(百澤安?)治療4周期。期間于2020-09-07至2020-09-25行胰腺病灶三維適形調強放療:預防區計劃靶區(PTV):2.0Gy×15f;原發腫瘤計劃腫瘤靶區(PGTV):2.4Gy×15f。客觀療效評估為部分緩解(PR)。治療后血清CA19-9降至正常范圍。
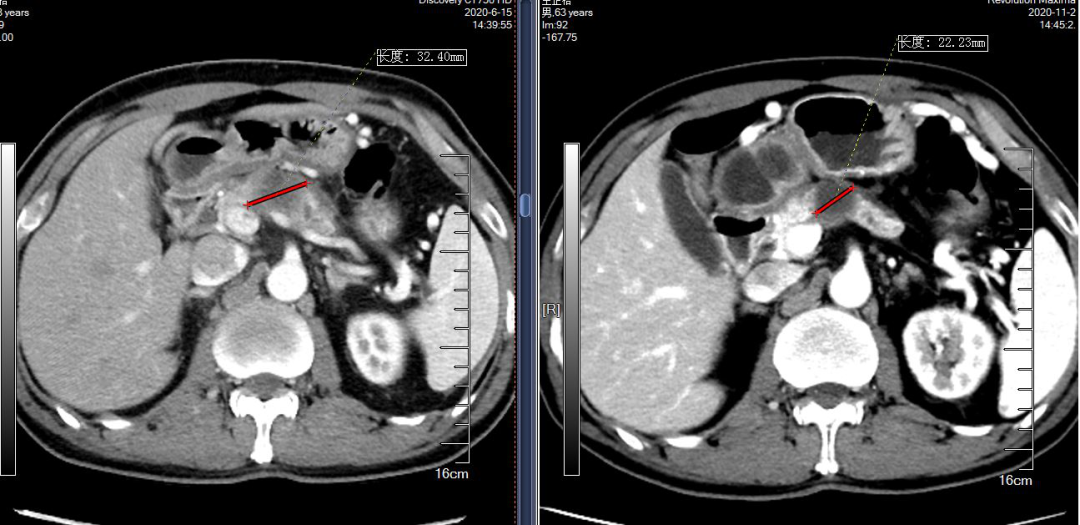
圖1 患者病灶治療前后的CT變化:治療前腫瘤最大徑32mm vs 化療4周期+放療1月后腫瘤最大徑22mm
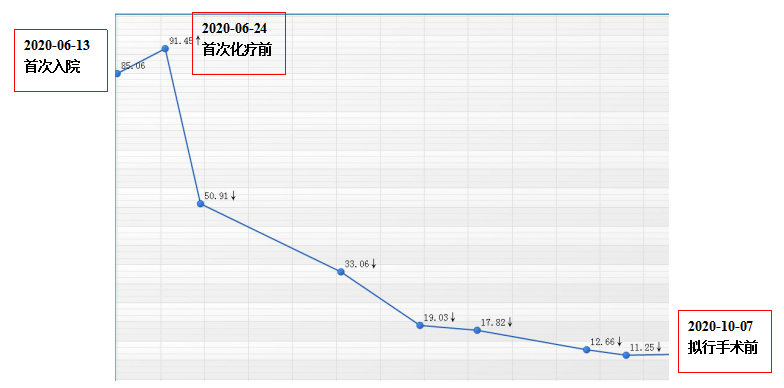
圖2 患者治療期間CA19-9變化趨勢
患者于2020-11-10行全胰十二指腸切除+全脾切除+遠端胃切除+門靜脈-腸系膜上靜脈切除+人工血管重建+區域淋巴結廓清+胰周神經切除+營養性空腸造瘺術。
術后病理:(全胰腺、部分胃及十二指腸切除標本):導管腺癌伴中-重度治療反應,膠原及退變壞死區域約占80%,殘余腫瘤細胞多位于病變周邊部,CAP評分:2分;Evans分級:2級。神經(+),脈管(-),切緣(-),淋巴結(0/10)。
分期:ⅡA(yT3,N0,cM0)。
免疫組化:癌細胞表達Ki67(40%+),P16(-),CD56(-),PD-1(淋巴細胞10個/HPF),PD-L1(SP142)(癌細胞1%+,間質免疫細胞2%),CD3(淋巴細胞60個/HPF+),CD8(淋巴細胞25個/HPF+)。

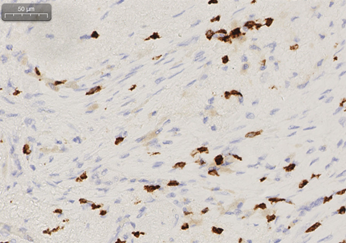
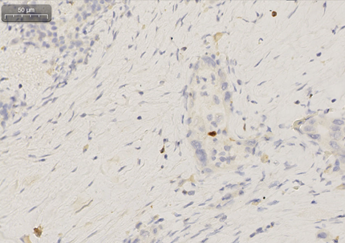
圖3 患者術后病理組織免疫組化(CD3、CD8、PD-1)
病例小結:
該患者為胰體部癌,合并門靜脈、腸系膜上靜脈及脾靜脈侵犯,為交界可切除腫瘤。經化療、放療聯合替雷利珠單抗免疫治療后,病灶明顯縮小,療效評價達PR,血清CA19-9降至正常。該患者轉化治療有效,遂進行手術,達到R0切除,術后出現胰瘺,無其他不良反應。術后病理示腫瘤壞死率高達80%,CD3、CD8免疫細胞比例高,PD-1表達高,考慮可能與替雷利珠單抗的使用有關。
專家病例點評
對于潛在可切除的胰腺癌,近年來越來越多的證據支持行術前新輔助治療。已有多項臨床研究報道,交界可切除或者局部晚期患者先行新輔助放化療后再手術,可以提高轉化率,增加行根治性手術的機會,提高R0切除率,減少術后肝轉移的風險,延長無病生存期和總生存期。2019年美國哈佛大學的一項研究證實,新輔助化療+放療可以使局部晚期胰腺癌受試者的R0切除率達到61%。但是NCCN指南中指出,目前關于新輔助治療的方案尚缺乏大樣本的III期臨床研究的數據,所以還沒有公認的放化療方案,因此建議在大型臨床醫學中心積極開展相應的臨床研究。
胰腺癌普遍被認為是免疫治療不敏感的瘤種,對于非錯配修復缺陷/微衛星高度不穩定(dMMR/MSI-H)或者非腫瘤突變負荷高(TMB-H)的患者,單用PD-1抗體免疫治療往往無效。胰腺與十二指腸和胃等空腔臟器毗鄰,由于這種解剖結構的特殊性,導致胰腺癌部位無法行大劑量放療,單純常規劑量的放療往往效果不佳。另外胰腺癌豐富的間質又使得化療藥物難以滲透,因此單純化療達到PR的也不多。化療和放療可以促進腫瘤抗原的釋放,改善腫瘤免疫微環境,激活機體免疫反應等,如果將免疫治療和化療、放療等有機組合后則會產生相對較好的結果,在胃癌、肺癌等其它瘤種均已見到相關治療的報道。
該病例經過化療聯合免疫治療序貫放療的新輔助治療后,病灶縮小達PR,血清腫瘤標記物CA19-9降至正常,之后的手術達到了R0切除。尤其令人感到可喜的是術后病理報告顯示腫瘤壞死達到80%以上,更令人感興趣的是,免疫組化顯示CD3、CD8等免疫活性細胞的比例顯著增多(與既往未行新輔助治療的患者的病理相比),考慮這可能是新輔助治療改善腫瘤微環境,激活免疫反應的一種表現。治療期間無明顯不良反應,患者耐受性良好。這種新輔助治療的模式值得在胰腺癌的治療中進一步探索。
總結
胰腺癌也被稱為“癌中之王”,中位生存期只有約3-6個月,5年生存期少于5%。化療仍然是晚期胰腺癌治療的基石,然而現有標準化療方案獲益有限。免疫治療為胰腺癌帶來了新的希望,但由于胰腺癌免疫抑制性的腫瘤微環境,限制了單純免疫治療的效果。近年來研究發現,免疫治療聯合化療具有協同效應,較單一化療方案可顯著延長患者OS,并且免疫治療聯合放療也顯示出初步療效。本例患者接受替雷利珠單抗免疫治療、聯合化療序貫放療的新輔助治療后,病灶縮小,手術達到R0切除,療效喜人。
替雷利珠單抗是由百濟神州自主研發的針對PD-1的人源化單克隆抗體,結構上對Fc段進行了獨特改造,去除了自身與巨噬細胞表面FcγR結合的能力,避免了抗體決定的細胞吞噬(ADCP)效應導致的T細胞消耗。其Fab段與PD-1的親和力高于同類抗體,發揮強大阻斷作用。目前,替雷利珠單抗已獲批用于復發/難治經典型霍奇金淋巴瘤和局部晚期或轉移性尿路上皮癌,其在胰腺癌中的應用前景值得關注。