離子的遷移速度由離子的電荷與大小決定。
離子的大小不是指凈尺寸,而是包括水合層的尺寸。水溶液中所有的離子都被極化的水分子所包圍。這意味著一個很小但高度水合的Li離子遷移速度比較大但微量水合的K離子的遷移速度慢。由于H+和OH-離子的遷移依據完全不同的機理,它們比其它任何的離子移動速度都快。不同離子的遷移速度可見圖25。
| 離子遷移率(10-4 cm2 / s·V),25℃時 | |||
| H+ | 36.25 | OH- | 20.64 |
| Li+ | 4.01 | F- | 5.74 |
| Na+ | 5.19 | Cl- | 7.91 |
| K+ | 7.62 | NO3- | 7.41 |
| NH4+ | 7.62 | CH3COO- | 4.24 |
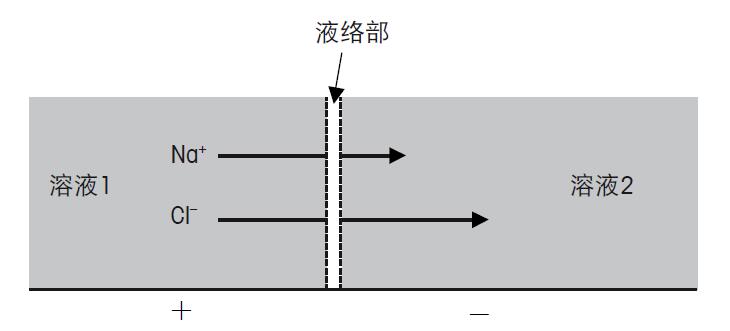
圖25.離子通過液絡部遷移、擴散
以鈉離子和氯離子為例,從表中可以看出鈉離子和氯離子從溶液1擴散至溶液2的速度不同。由于Cl-的遷移速度快于Na+,就會發生電荷分離。
電荷分離會產生擴散電位,擴散電位能抵消初始的遷移。這樣的交替會導致一個動態的平衡,需要很長的時間才能穩定。這意味著不同的離子擴散速度會造成電極響應時間緩慢。所以保持液絡部的電解液的高滲透性非常重要,可以盡量減短響應時間。
當陰離子與陽離子的遷移速度差別很大時,電荷分離和擴散電位就會上升。這個現象在強酸和強堿溶液中特別明顯,pH測量時經常遇到此類樣品。另一個決定Ediff的因素是溶液是否非常的稀。典型的例子是測量離子缺乏型的樣品如純水。
由于液絡部外的離子缺乏型樣品增強了電荷的落差,擴散電位會加強。
為了盡量減少擴散電位,必須保證使用高濃度并等遷移(陰陽離子遷移速度一致)的參比液。這就是為什么通常使用KCI和KNO3作為參比液,請見圖25。
盡管有了這些預防措施,使用了理想的參比電極,但在測量極限pH時,擴散電位仍然不能忽視。
下面的例子證明了這個現象(25℃):
| 內電解液 | 樣品溶液 | 擴散電位 | ΔpH |
| KCl (飽和) | HCl (1 mol/L) | Ediff = + 14.1 mV | 0.238 pH單位 |
| KCl (飽和) | NaOH (1 mol/L) | Ediff = - 8.6 mV | 0.145 pH單位 |
擴散電位的描述,更好解釋了測量一些樣品的pH非常的困難。測量稀溶液或離子缺陷型溶液如非水溶液,需要特別的注意。這種情況中的擴散電位會非常高,會導致不穩定的參比信號。因為會抑制電解液的順利滲出,污染的液絡部也會有這種現象。
4.5 pH測量的校準/調節設置
儀表中有兩種與連在儀表上的具體電極相關聯,并且在調節pH電極和儀表設置時會受到影響的設置,分別稱為電極的零點漂移(mV)和斜率(mV/pH)。由于有兩方面需要校準,所以應執行最少兩點校準。
校準零點和斜率可以補償實際值與理論值的偏移。偏移是由非理想狀況的電極產生的。大多數玻璃pH電極,pH7.00的緩沖液相應于零電位,并被用于零點校準。大多數情況下,考慮到待測樣品的pH范圍,可推薦pH4.01或pH9.21(或10.00)的緩沖液用于斜率校準。
下面的圖中,圖解了這兩方面的校準。左圖為零點校準,表示了與理論0mV(pH7.00時)的偏移。右圖為斜率的校準,表示了與理論59.16 mV/pH(25℃)的偏移。
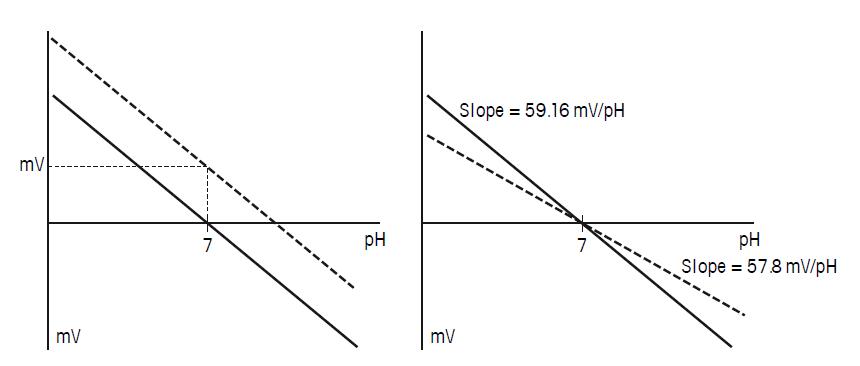
圖26. 左:pH電極零點校準,右:pH電極斜率校準。實線為理想的狀況,虛線為實際的狀況。
4.6 溫度對pH測量的影響
溫度對電極和樣品都會產生影響。本節將就此影響作詳細的分析。
溫度對電極的影響
溫度對電極的影響有以下幾個方面:
斜率
Nernst 方程給出了對于pH電極測量電位與樣品pH值的關系,可以看出這個斜率包含了開氏溫度:
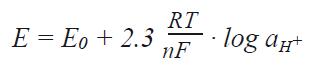
當帶入除了開氏溫度(T)外的所有數字,可以得到:
E = E0 –0.198 · T · pH
從這個方程中,可以清楚地看出電極的斜率與溫度呈線性關系。由于此線性關系可以預測,所以可以通過pH儀表和帶有溫度探頭的電極進行補償。
等溫點
每一支電極都有其自身的等溫點,等溫點由電位E1至E6所決定。理想電極,不同溫度的校準線都應在零點交叉(pH 7.00/0 mV),而且斜率應與絕對溫度呈一定的比例。
由于pH電極的總電位由E1-E6的總合組成,其中每一個電位對溫度有其各自的關系,所以等溫點通常不會與電極的零點一致。
電極的等溫點應盡量與零點接近,因為等溫點越是接近pH7,溫度補償的誤差就越小。
校準溫度與樣品溫度差別越大,測量誤差就越大,誤差最大約有0.1pH。為了得到最精確的pH測量值,應保持校準與樣品溶液溫度相同。
測量誤差請見圖27.
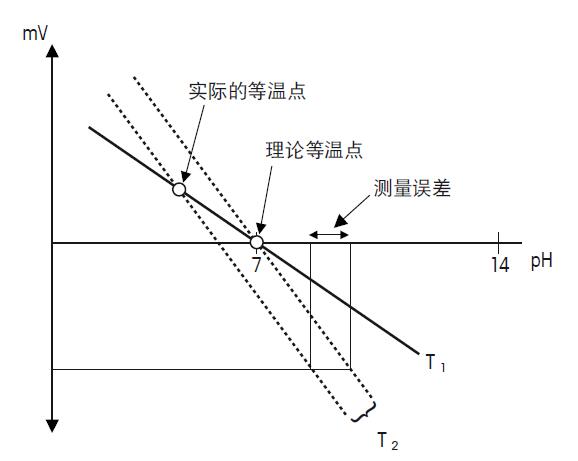
圖27. 理論與實際的等溫點
如果實際等溫點與理論的不一致,若樣品與樣品間或樣品與校準間的溫度相差過大,會造成較大的測量誤差。
此外,如果實際等溫點遠遠偏離理論等溫點,并且測量校準在不同的溫度下,誤差會非常的嚴重。