病例資料
患者,男,65歲,因“反復皮疹6年,尿檢異常3年,血清肌酐(SCr)升高1年”于2015-10-15入院。2009年患者飲酒后出現雙下肢皮膚出血點,大小不一,壓之不褪,以左下肢明顯,至當地醫院檢查考慮“過敏性紫癜”,未行尿檢,具體治療方案不詳,皮疹緩解,此后飲酒或食用辛辣食物后反復出現雙下肢皮疹,未重視。2012年尿檢發現尿蛋白陽性(具體不詳),腎功能不詳,服潑尼松30 mg/d,后自行減至20 mg/d,尿蛋白持續陽性。2014年8月出現雙下肢水腫,當地醫院查血壓偏高,最高達160/100 mmHg,尿蛋白+++,血清白蛋白(A1b)27.4 g/L,SCr 154 μmol/L,行腎穿刺活檢術提示“假性膜增生性過敏紫癜性腎炎(IsKDⅣ型)”,予潑尼松、雷公藤多苷及硝苯地平緩釋片治療,血壓控制不佳,未復查。2015年9月復查SCr升至408.5 μmol/L,血紅蛋白78 g/L。2015年10月至我院門診查尿蛋白定量5.75 g/24h,尿沉渣紅細胞240 萬/ml,尿白細胞(WBC)10~15 個/HP,尿糖+++,Alb 34.4 g/L,SCr 385 μmol/L,空腹血糖7.35 mol/L,補體C3偏低(O.6 g/L),C4正常,cANcA、pANCA陰性,雙腎體積可、結柯欠清。1月前曾有1次痰中帶血絲,未經處理自行緩解,無肉眼血尿、關節痛,無咳嗽、咳痰,無胸悶、氣喘,無頭暈、頭痛,無腹脹、腹瀉、腹痛、黑便、脫發、頻發口腔潰瘍。患者目前常有惡心、嘔吐感,精神、體力正常,食欲較差,睡眠可,近期體重明顯變化,大便正常,尿量正常。既往史40年前曾行“闌尾切除術”,2014年曾行“痔瘡切除術”。
體格檢查血壓113/73 mmHg,全身無明顯皮疹,心肺腹體檢未及明顯無異常,雙下肢無水腫。
實驗室檢查
尿液尿蛋白定量5.75 g/24h,尿沉渣紅細胞計數240 萬/ml(80%多形型),尿WBC 0-1 個/HP;尿糖++;尿C3 10 mg/L;尿α2-MG 4 mg/L;尿NAG 50.4 U/(g.cr),RB蛋白 58.2 mg/L,溶菌酶61.54 mg/L。血紅蛋白74 g/L(正細胞正色素性貧血),網織紅細胞33.6×109/L,網織紅細胞比例1.18%,白細胞9.3×109/L,血小板175×109/L。Alb 30.4 g/L,球蛋白14.1 g/L,SCr 302 μmol/L,BUN 8.6 mol/L,UA 252 μmol/L,A1月14 U/L,AST 16 U/L,總膽固醇4.44 mmol/L,三酰甘油0.92 mmol/L,鈣2.18 mmol/L,其余電解質正常,空腹血糖4.9 mmol/L,餐后血糖8.O mmol/L,HbAlc 5.4%。eGFR 17.80 ml/min/1.73m2(采用EPI公式計算)。IgA 3.78 g/L(正常值O.7~4.0 g/L),IgG 1.43 g/L(正常值7~16 g/L),IgM 0.185 g/L(正常值O.4-2.3 g/L),類風濕因子及抗鏈“0”正常,ANA、A—dsDNA、pANCA、cANCA、抗GBM抗體陰性。血游離輕鏈κ 92.29 mg/L,λ30.06 mg/L,κ/λ=3.07。血清免疫固定電泳未見單克隆免疫球蛋白條帶。補體C3 0.60 g/L,C4 0.19 g/L,C3腎炎因子陰性,補體H因子正常、抗補體H因子抗體陰性。乙型肝炎病毒表面抗原、表面抗體、e抗原無異常,e抗體O.79,核心抗體8.41。丙型肝炎病毒IgG抗體、抗HIV抗體、抗梅毒螺旋體抗體均陰性。
輔助檢查
胸片左上肺結節。心電圖大致正常心電圖。腹部平片(1)腹主動脈鈣化總積分為0分;(2)腰椎退行性變。CT冠狀動脈鈣化分數測定左冠狀動脈前降支可見鈣化,鈣化總積分為32.6。心臟超聲:(1)主動脈瓣鈣化伴輕度反流。(2)輕、中度二尖瓣反流。腎臟超聲:左腎93 mm×41 mm×46 mm,右腎96 mm×46 mm×48 mm,腎皮質厚度不清,腎皮質回聲稍增強,皮髓界限清楚,集合系統正常,右腎中極見一大小約9 mm×9 mm類圓形無回聲區,雙腎輪廓規則,包膜連續完整,雙腎內未見腎盂腎盞擴張。骨髓穿刺細胞學檢查輕度血稀骨髓象,漿細胞占1.5%,為成熟漿細胞;骨髓活組織檢查:右側髂前上棘示骨髓增生活躍。
腎活檢病理
光鏡:皮質腎組織l條。35個腎小球中14個球性廢棄(40%)。余腎小球系膜區中、重度增寬,毛細血管袢開放尚好,節段袢內皮細胞增殖,單個核細胞浸潤致數處袢腔狹小,偶見PAs弱陽性的“栓子”(圖1A),囊壁節段增厚。PASM-Masson:腎小球系膜區節段、內皮下較多、上皮側偶見嗜復紅物沉積(圖lB),較多外周袢分層(圖1C)。腎小管間質慢性病變中度,灶性腎小管萎縮、基膜增厚,未萎縮腎小管基膜亦增厚,急性病變中度,多灶性腎小管上皮細胞刷狀緣脫落,管腔內見蛋白管型、紅細胞管型及脫落的腎小管上皮細胞,間質彌漫單個核細胞浸潤,散在泡沫細胞分布,灶性纖維化++。小葉間動脈內膜增厚,小動脈節段透明變性。

圖1 (A)腎小球系膜區中一重度增寬,毛細血管袢腔狹小,偶見“栓子”(箭頭)(PAs ×400);(B)腎小球系膜區、內皮下、上皮側嗜復紅物沉積(箭頭)(Masson三色 ×400);(C)腎小球外周袢分層(箭頭)(PASM-Masson ×400)
免疫熒光
17個腎小球,IgA++(圖2A)、IgMtrace、C3++、κ輕鏈++(圖2B)、λ輕鏈++(圖2C),呈顆粒狀彌漫分布于系膜區及血管袢,以血管袢沉積為主。IgG、C1q陰性。電鏡3個腎小球。腎小球系膜區增寬,系膜細胞及系膜基質增多,系膜區見密度不均的電子致密物分布(圖3A);腎小球毛細血管袢開放欠好,袢腔內充填腫脹、增生的內皮細胞及浸潤細胞(單核細胞、淋巴細胞及中性粒細胞);多處系膜插入、新的基膜形成。低倍鏡下毛細血管袢基膜內皮下節段、上皮側偶見密度不均勻的電子致密物沉積(圖3B),高倍鏡下致密物為中空微管狀結構,直徑33-47 nm,平行排列(圖3C)。腎小球毛細血管袢基膜厚度約250~410 nm。腎小球足細胞足突廣泛融合(70%~80%),胞質少量微絨毛化,胞質內見吞噬性溶酶體。
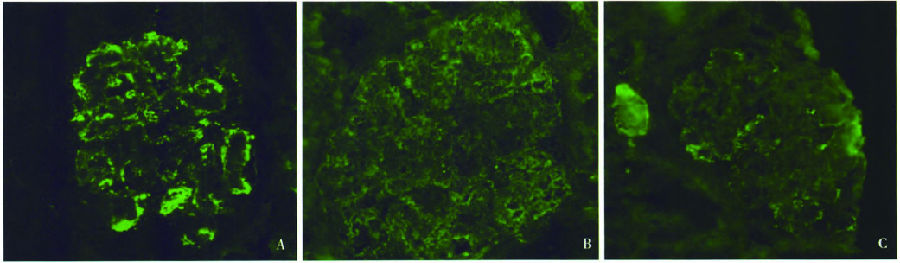
圖2 IgA ++(A),κ ++(B),λ ++(C),呈顆粒狀沉積于腎小球系膜區及血管袢,并以血管袢沉積為主(IF ×400)

圖3 (A)腎小球系膜區、基膜內皮下及上皮側見密度不均勻的電子致密物沉積;(B、C)高倍鏡下致密物為中空微管狀結構直徑33-47 nm,平行排列(EM)
診斷
IgA型免疫管狀腎小球病
討論
患者為老年男性,慢性病程,臨床表現腎病綜合征,大量鏡下血尿,腎功能不全及高血壓;腎外表現為反復發作的雙下肢紫癜樣皮疹,補體C3偏低;血液系統表現為貧血,IgA水平正常但IgG、IgM明顯下降,血輕鏈κ/λ比例增高,骨髓細胞學示成熟漿細胞1.5%。腎活檢光鏡改變為腎小球膜增生樣病變(MPGN)伴袢腔內偶見“栓子”,免疫熒光以IgA、C3血管袢沉積為主,電鏡下沉積物為微管狀物質。
MPGN根據免疫病理可分為免疫復合物相關腎小球疾病、單克隆免疫球蛋白相關的腎小球疾病和C3腎病。該例患者免疫熒光除C3外,同時存在免疫球蛋白IgA沉積,IgA和C3染色強度相等,排除C3腎病的診斷。其次,患者自身抗體陰性、無丙肝病毒及活動性乙肝病毒感染、無患實體腫瘤證據,排除自身免疫、感染、實體腫瘤相關的免疫復合物介導的腎小球疾病。免疫球蛋白染色IgA++,IgM trace,IgG陰性,結合患者血液系統的表現,應積極排查單克隆免疫球蛋白相關的腎小球疾病。進一步行輕鏈染色示腎小球κ、λ均陽性,但是,在IgM陽性的情況下,不能完全根據輕鏈染色雙陽性而否定單克隆免疫球蛋白相關的腎小球疾病。。
免疫熒光腎小球以IgA沉積為主的疾病,常見有以下幾類疾病。(1)IgA腎病:光鏡下的表現呈多樣性,從腎小球輕度系膜增生性病變至彌漫增生性病變,免疫熒光IgA系膜區沉積為主,電鏡下電子致密物無特殊結構。腎外無皮膚紫癜的表現,因此本例患者不考慮IgA腎病。(2)過敏性紫癜性腎炎:與IgA腎病的光鏡、免疫熒光及電鏡相類似,國際腎臟病組織(IsKD)將其分為六型,其中Ⅵ型為“腎小球膜增生樣病變”。腎外表現為皮膚紫癜,較常見于雙下肢伸側,補體C3水平正常。該例患者盡管存在紫癜樣皮疹,但IgA沉積的部位以血管袢為主,且最為突出的表現為電鏡下沉積物具有特殊結構,與過敏性紫癜性腎炎的免疫熒光及超微結構特點均不符。(3)IgA沉積為主的感染后腎小球腎炎:常見于中老年人,糖尿病為易患因素,多為葡萄球菌感染誘發,補體C3下降,光鏡主要表現腎小球彌漫毛細血管內細胞增殖性病變伴顯著的中性粒細胞浸潤,免疫熒光以IgA、C3沉積為主,且C3染色多強于IgA,電鏡見典型“駝峰”形成舊J。該例患者無糖尿病,起病前無感染誘因,電鏡下亦未見“駝峰”形成,因此不符合。(4)IgA沉積為主的MPGN,本例患者屬于此類,進一步行電鏡及其他輔助檢查有助于明確診斷。
本例患者電鏡下觀察發現超微結構極具特征性,表現為低倍鏡下腎小球系膜區、毛細血管袢基膜內皮下較多、上皮側偶見密度不均勻的電子致密物沉積,高倍鏡下電子致密物呈中空微管狀結構,直徑均一,約33~47 nm,平行排列。根據該超微結構特點,結合光鏡及免疫熒光,診斷考慮免疫管狀腎小球病。
免疫管狀腎小球病的光鏡主要表現為MPGN,可伴內皮下大量沉積物,少數可見袢內栓塞形成,其次為腎小球膜性病變和腎小球毛細血管內增生性病變,沉積物PAS弱陽性、嗜伊紅、不嗜銀,一般不累及腎小管間質及血管。免疫熒光免疫球蛋白以IgG沉積多見,IgA、IgM少見,目前報道的病例中以單克隆性的單一重鏈及單一輕鏈常見。電鏡下沉積物為平行或成束排列、無分枝、直徑均一,約20~90 nm、多數30~60 nm的中空微管狀物。目前它的診斷標準為:(1)免疫熒光免疫球蛋白沉積,(2)電鏡<30 000放大倍數下可見中空微管狀結構,(3)局部或全部呈平行排列,(4)排除冷球蛋白相關腎小球腎炎及狼瘡性腎炎。
IgA型免疫管狀腎小球病極為罕見,目前僅見個案報道。免疫管狀腎小球病需要鑒別其他免疫球蛋白沉積伴電鏡下具有特殊超微結構的疾病,包括系統性淀粉樣變性、冷球蛋白血癥腎小球腎炎、單克隆免疫球蛋白沉積的增生性。腎小球腎炎、纖維性腎小球腎炎等。免疫球蛋白通常為IgG,以IgA沉積為主病例盡管罕見,但不能忽視。(1)重鏈及輕-重鏈型淀粉樣變性:腎組織剛果紅染色陽性,腎小球、血管、間質、腎小管基膜均可沉積,淀粉樣物質PAS及銀染可呈陽性,免疫熒光單一重鏈IgA及單一的κ或λ沉積,電鏡下為無分枝、排列紊亂、直徑8~12 nm的纖維絲,無微管狀結構。(2)冷球蛋白血癥相關性腎小球腎炎:血冷球蛋白陽性,光鏡下呈MPGN,袢腔內可見PAs強陽性的冷球蛋白栓子,超微結構可見彎曲微管狀、桿狀、纖維絲狀、指紋狀結構,但不是每例冷球蛋白血癥的患者沉積物均具有超微結構,本例患者超微結構的微管狀物與冷球蛋白的不同,呈平行排列,需待冷球蛋白結果進一步排除。有研究報道IgA型冷球蛋白血癥相關的腎小球腎炎,腎臟病理為腎小球彌漫毛細血管內滲出性病變,IgA沉積于腎小球系膜區、內皮下,以及袢腔內形成“栓子”,電鏡下電子致密物為“網格狀”晶體(縱切面為20 nm寬條紋,橫切面為直徑10 nm的微管)。(3)單克隆免疫球蛋白沉積的增生性腎小球腎炎:免疫病理腎小球單一的重鏈亞型和單一輕鏈沉積,腎小管、間質及血管壁陰性。(4)纖維性腎小球腎炎:光鏡為腎小球系膜增生性病變伴袢壞死及新月體,免疫熒光腎小球IgA及單一κ輕鏈沉積,電鏡下可見系膜區、基膜膜內、內皮下及上皮側無分枝的、短直的纖維絲,最長200 nm,直徑10~23 nm,無微管狀結構,排列紊亂或偶見成對平行排列。
本例患者腎臟表現為腎病綜合征及腎功能不全,同時存在補體C3下降,貧血,IgA水平正常但IgG、IgM水平明顯下降,血輕鏈比值異常,骨髓細胞學成熟漿細胞占1.5%,考慮為漿細胞相關性疾病。患者隨訪9個月時,進人維持性血液透析。此外,本例患者極具迷惑性的臨床表現為病程中反復出現皮膚紫癜,腎小球腎炎合并紫癜樣皮疹的鑒別診斷中,最常見的疾病為過敏性紫癜,其皮膚活檢可見IgA沿血管壁沉積,其次,冷球蛋白血癥患者也可出現紫癜樣皮疹。免疫管狀腎小球病伴有紫癜樣皮疹的病例報道僅有3例,皮膚活檢均為白細胞破碎性血管炎,皮膚血管周圍伴或不伴免疫球蛋白沉積。對于紫癜樣皮疹,有條件應行皮膚活檢行光鏡和免疫熒光染色有助于鑒別診斷。免疫管狀腎小球病的發病機制尚未明確,激光微分離腎小球質譜分析提示微管狀沉積物的成分為免疫球蛋白、補體,并含淀粉樣P物質、載脂蛋白E等。
總之,本例是極為罕見的IgA型免疫管狀腎小球病,光鏡表現為MPGN,免疫熒光IgA血管袢沉積為主,電鏡下腎小球系膜區、內皮下、上皮側見極具特征性的平行排列的中空微管狀的超微結構。臨床表現。腎病綜合征和大量鏡下血尿,伴補體C3下降、貧血、IgA水平正常但IgG、IgM水平明顯下降,血輕鏈比值異常,病程中反復發作紫癜樣皮疹,需要長期隨訪排除漿細胞異常增生性疾病或其他特殊疾病。腎小球以IgA沉積為主的疾病病因多樣,需結合臨床考慮,電鏡是診斷和鑒別診斷的重要手段。